Postagem relacionada
Crio-EM: Visualizando Biomoléculas em Resolução Próxima à Atômica
2026-02-21Cryo-EM: Visualizar Biomoléculas em Resolução Próxima à Atômica está remodelando a biologia estrutural porque ajuda pesquisadores a observar proteínas, complexos e vírus em condições mais próximas da vida real — sem cristais exigentes ou manuseio excessivamente agressivo das amostras. A Longlight Technology apoia projetos de criomicroscopia eletrônica com fluxos de trabalho claros, entregas transparentes e orientações práticas que ajudam as equipes a passarem de "uma amostra promissora" para "uma estrutura defensável" mais rápido e com menos becos sem saída.
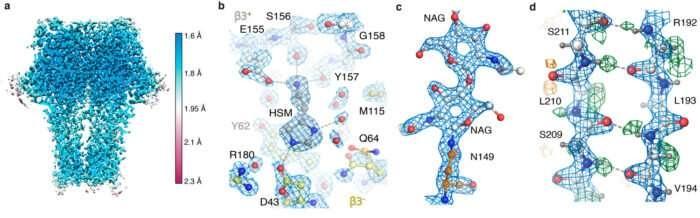
Cientistas quebram recordes de resolução para visualizar átomos individuais com crio-EM de partícula única
Em vez de tratar o crio-EM como um serviço misterioso e de alto nível que só funciona para amostras perfeitas, abordamos como um sistema de decisão estruturado: analisar o que você tem, aprender o que está fazendo e só escalar para coleta de dados em alta resolução quando a amostra estiver realmente pronta. Essa mentalidade economiza tempo, orçamento e material precioso — especialmente para usuários de primeira viagem que precisam de resultados que sobrevivam à revisão interna e por pares.
Por que a crio-eletroeletromagnética é importante para a biologia estrutural moderna
O que é Cryo-EM
Crio-EM (crio-microscopia eletrônica) é uma forma de "ver" moléculas biológicas ao imagiá-las com um microscópio eletrônico após congelá-las rapidamente em uma fina camada de gelo vítreo (semelhante a vidro). O congelamento prende moléculas em um estado quase nativo sem fixação química ou cristalização, e computadores combinam muitas visões 2D para reconstruir uma estrutura 3D — muitas vezes em resolução próxima à atômica para amostras bem comportadas.
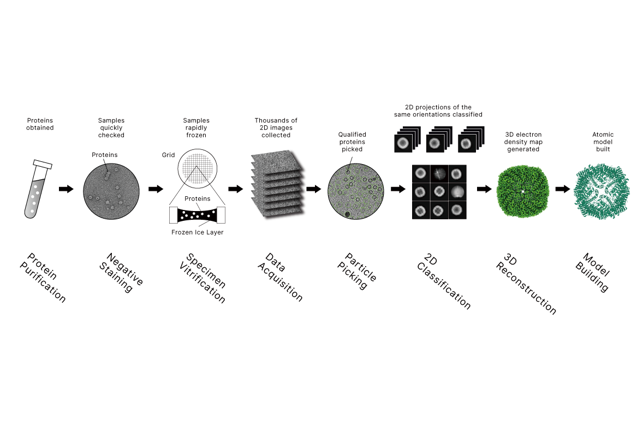
How Cryo-EM Works (Simple View)
• Preparar a amostra (proteína, complexo, vírus, etc.) em solução
• Vitrificá-lo congelando rapidamente para que a água se torne gelo parecido com vidro (sem cristais de gelo)
• Imageie de milhares a milhões de partículas usando um microscópio eletrônico de transmissão
• Calcular: alinhar, classificar e reconstruir um mapa 3D; às vezes construir um modelo atômico
Principais Métodos de Crio-EM
• Análise de Partícula Única (SPA): melhor para proteínas/complexos purificados; Resoluções mais altas são comuns aqui.
• Tomografia Crio-Eletrônica (Crio-ET): Imagem 3D de estruturas em células ou ambientes nativos; Ótimo para contexto espacial.
• Microdifração de Elétrons (MicroED): para cristais muito pequenos (nano/microcristais) quando a cristalografia é difícil.
Por que as pessoas escolhem o Cryo-EM
• Não há necessidade de crescer cristais
• Captura moléculas mais próximas ao seu estado nativo
• Funciona bem para grandes complexos e muitos alvos "difíceis"
• Pode revelar múltiplos estados estruturais (movimento/flexibilidade)
Nas ciências da vida, a maneira mais rápida de entender uma biomolécula é frequentemente observar sua forma e como essa forma muda. O Cryo-EM torna isso possível para alvos que são difíceis, flexíveis ou instáveis — exatamente os alvos que muitas equipes mais valorizam. A microscopia eletrônica criogênica se baseia na microscopia eletrônica de transmissão e pode reconstruir estruturas 3D desde resolução subnanômica até quase atômica, dependendo do comportamento da amostra e da qualidade dos dados.
Isso é especialmente valioso em áreas de alto impacto onde detalhes orientam as decisões:
• Descoberta de medicamentos: bolsões de ligação, geometria da interface e alterações induzidas no ajuste
• Anticorpos e vacinas: mapeamento de epítopos, mecanismos de neutralização e estabilidade complexa
• Virologia: organização da capside, mudanças conformacionais e vias de montagem
• Proteínas de membrana: canais, transportadores, receptores e complexos de múltiplas passagens
Muitos alvos modernos não cristalizam facilmente, e alguns nunca o farão. O Cryo-EM frequentemente converte "isso é difícil demais de cristalizar" em "isso já pode ser testado", porque o fluxo de trabalho é feito para iteração: você faz uma triagem rápida, ajusta as condições de forma inteligente e depois aumenta a escala quando as partículas se comportam.
Crio-EM vs Cristalografia de Raios-X: O que iniciantes devem saber
A cristalografia de raios X continua sendo um método poderoso e pode alcançar resolução extremamente alta no caso certo. Mas se você é novo no planejamento de projetos em biologia estrutural, ajuda focar em risco e probabilidade, não apenas na resolução máxima teórica.
O Cryo-EM reduz vários bloqueadores comuns de projetos:
• Não é necessária cristalização, o que elimina uma grande incerteza
• Estado quase nativo preservado em gelo vitrificado, melhorando a relevância biológica
• Alvos flexíveis ou dinâmicos podem ser avaliados em vez de "fazer a média"
• Alvos difíceis tornam-se mais viáveis (proteínas de membrana, grandes conjuntos, vírus)
• A heterogeneidade pode, às vezes, ser separada computacionalmente em estados distintos
• Menor tolerância à pureza pode ser possível para amostras de descoberta precoce (dependendo do caso)
• Menor desperdício de amostra em comparação com a triagem de cristalização repetida
Uma forma simples de pensar sobre isso: a cristalografia pode ser extraordinária quando a cristalização funciona, mas a crio-EM costuma ser o caminho mais previsível para alvos difíceis, complexos multicomponentes e projetos onde você não pode se dar ao luxo de meses de tentativa e erro.
Comparação entre Cristalografia de Raios X, RMN e EM - Bioestrutura Criativa
Soluções Estruturais que Oferecemos: De Cribragem a Modelos Quase Atômicos
Na Longlight Technology, nossa estrutura de serviço crio-EM corresponde ao progresso dos projetos reais. Agrupamos o trabalho em três objetivos práticos — para que seu caminho se encaixe na sua amostra e na pergunta que você está tentando responder.
Avaliação de Adequação da Amostra com Triagem Negativa por Manchas
Antes de investir em grades criogênicas e tempo de microscópio de alta qualidade, a triagem negativa de manchas atua como um choque de realidade. Normalmente é feito em temperatura ambiente e ajuda a responder a primeira pergunta que importa: a amostra se comporta como uma amostra estrutural?
A mancha negativa pode revelar:
• agregação ou agrupamento
• integridade e morfologia das partículas
• distribuição de tamanho e adequação à concentração
• heterogeneidade grosseira (muitas "formas" ao mesmo tempo)
• sinais de instabilidade ou degradação
Pense no verniz negativo como um portão de qualidade. Não é para publicar mapas em alta resolução. Ele tem como objetivo evitar a coleta cara de dados em uma amostra que ainda não está pronta — e orientar a próxima etapa de otimização com evidências em vez de suposições.
Determinação de estrutura em alta resolução com análise de partícula única
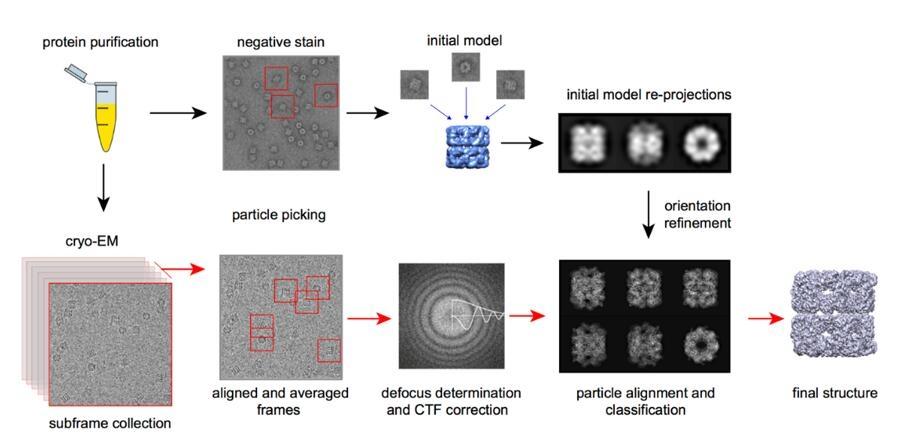
Para muitas proteínas e complexos solúveis, a análise de partícula única (SPA) é o caminho mais comum para resultados de alta resolução. Grandes conjuntos de dados contêm vistas individuais de partículas de várias orientações. O processamento computacional alinha e classifica essas imagens de partículas e reconstrói um mapa de densidade 3D. Quando o mapa permite isso, um modelo atômico pode ser construído e refinado para revelar mecanismos invisíveis apenas para leituras bioquímicas.
É onde o Cryo-EM: Visualizando Biomoléculas em Resolução Próxima à Atômica se torna diretamente acionável: interfaces de ligação, movimento de domínios e explicações estruturais para atividade, inibição ou especificidade podem ser descritos com confiança.
Análise estrutural in situ com tomografia crio-eletrônica
Se sua pergunta não é "como é essa partícula purificada", mas sim "como ela é organizada no contexto", a criotomografia eletrônica (Cryo-ET) é uma escolha melhor. A tomografia pode visualizar estruturas em um ambiente mais nativo, o que é útil para:
• Conjuntos associados à membrana
• grandes complexos celulares
• Organização de interação vírus-hospedeiro
• Questões sobre arranjo espacial e arquitetura
Crio-ET é frequentemente escolhido quando a história espacial importa tanto quanto a forma molecular.
Nosso Fluxo de Trabalho de Serviço e o Que Você Recebe
Um projeto crio-EM não deve parecer uma caixa preta. Colocamos clareza em cada etapa para que você sempre saiba o que está acontecendo, o que foi observado e quais decisões estão sendo tomadas.
Fluxo de trabalho típico:
Consultoria de Projeto → Assinatura → Confirmação do Acordo de Serviço → Recebimento → Amostra, Inspeção de Qualidade → Triagem de Manchas Negativas → Coleta de Dados Crio-EM → Processamento de Dados → Entrega de Relatórios
Os entregáveis são estruturados para uso real em pesquisa, não apenas para "uma boa imagem". Dependendo do escopo, você pode receber:
• Filmes crus crio-EM (com arquivos de referência de ganho quando aplicável)
• Saídas intermediárias chave de processamento
• Mapas finais de densidade 3D com métricas de resolução e qualidade
• Modelos de coordenadas atômicas (quando a densidade permite a construção de modelos)
• Relatórios de validação e cruzamento (por exemplo, avaliações de qualidade estrutural)
• Entrega organizada de dados via nuvem segura ou armazenamento portátil
O objetivo é simples: você deve ser capaz de reproduzir o trabalho, reprocessar se necessário e publicar com confiança — sem ficar atrás de arquivos depois ou se perguntar como as conclusões foram alcançadas.
Plataformas de Equipamentos que Combinam com Diferentes Estágios do Projeto
Amostras diferentes exigem diferentes níveis de potência e estratégia do instrumento. Pagar por um sistema principal para responder uma pergunta básica de triagem é ineficiente e frequentemente atrasa projetos.
Nossa capacidade de serviço crio-EM é suportada por plataformas que cobrem triagem por meio da determinação de estruturas de alta resolução, tais como:
• Talos L120C G2: triagem e avaliação eficiente de TEM/crio-EM
• Glacios 2 (200 kV): sistema robusto para fluxos de trabalho rotineiros de SPA e crio-ET
• Titan Krios G4 (300 kV): plataforma principal projetada para estabilidade, automação, throughput e potencial de resolução de alto nível
Essa abordagem em camadas apoia um princípio prático: use o microscópio certo no momento certo. A triagem permanece eficiente, e a coleta em alta resolução ocorre apenas quando a amostra está pronta para justificá-la.
Requisitos Práticos do Projeto, Prazos de Entrega e um Próximo Passo Claro
Se você está planejando seu primeiro projeto estrutural, detalhes de preparação de amostras são importantes. A maioria dos atrasos não é causada pelo "microscópio", mas por problemas evitáveis da amostra, como instabilidade, agregação ou componentes tampão incompatíveis.
Orientação típica de amostra mínima:
• Coloração negativa: ~1 g/L, ~100 μL
• SPA (proteínas solúveis): ~1 g/L, ~100 μL
• SPA (proteínas de membrana): ~1 g/L, ~100 μL (frequentemente ajustável por discussão)
Orientação típica de amortecedores:
•pH 6,0–8,5
• Concentração de sal <200 mM
• Preferência de baixo glicerol e baixa azida (otimização caso a caso é possível)
Janelas típicas de entrega:
• Triagem negativa de manchas: 1–2 semanas
• Desfechos preliminares da SPA: 6–8 semanas
• Modelo de alta resolução SPA (quando possível): ~2–3 meses
CTA: Se você quiser reduzir o risco de um novo alvo rapidamente, comece com a triagem negativa de manchas. Envie à Longlight Technology os detalhes da amostra (tipo de alvo, tampão, concentração e pureza estimada), e recomendaremos a rota mais eficiente — coloração negativa, SPA ou crio-ET — com base no seu objetivo científico e cronograma.
Por fim, muitos estudos crio-EM conectam-se à biologia upstream e downstream. A Longlight Technology também apoia fluxos de trabalho mais amplos de biologia molecular e genômica, incluindo instrumentos relacionados a NGS (como ultrasonicação focada) e consumíveis e kits comumente usados (géis de agarosa pré-moldados, kits de extração de ácidos nucleicos e kits de preparação de biblioteca), para que seu trabalho estrutural possa se conectar suavemente à descoberta, validação e design de estudos prontos para publicação.