Postagem relacionada
Espectrometria de Massa de Cross-Linking: Perguntas Frequentes e Soluções Comprovadas
2026-01-15A Espectrometria de Massa de Reticulação Cruzada amadureceu rapidamente, deixando de ser uma técnica especializada para se tornar uma pedra fundamental da proteômica estrutural e do mapeamento de interactomas. Inovadores iniciais, incluindo Ruedi Aebersold, Juri Rappsilber, Andrea Sinz e colaboradores, mostraram como o XL-MS pode validar modelos crio-EM, resolver a organização de grandes máquinas macromoleculares e expor contatos fugazes entre proteínas que raramente sobrevivem à purificação. Aproveitando esse impulso, nosso ecossistema integrado de serviços, instrumentos e consumíveis oferece fluxos de trabalho reproduzíveis e de alta capacidade para Espectrometria de Massa de Reticulação Cruzada – desde o planejamento de amostras até a interpretação de dados – projetados para atender às demandas da descoberta moderna. A Espectrometria de Massa de Reticulação (XL-MS) evoluiu para uma ferramenta central para proteômica estrutural e análise de interectomas. Ao capturar restrições espaciais entre resíduos, o XL-MS complementa crio-EM e cristalografia e revela interações transitórias proteína-proteína que frequentemente escapam de métodos baseados em purificação.
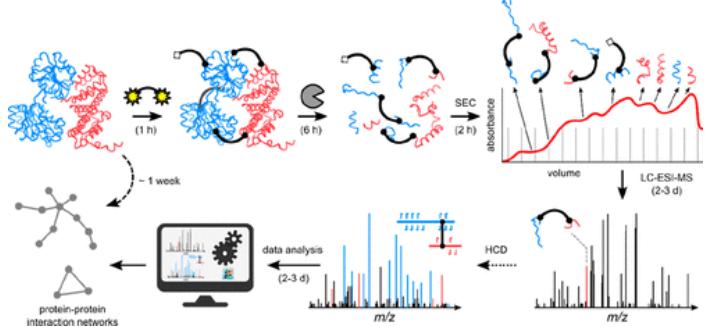
(Espectrometria de massa de reticulação cruzada para investigar conformações de proteínas
e Interações Proteína-Proteína - Um Método para Todas as Estações)
O que a espectrometria de massa de reticulação realmente captura
A Espectrometria de Massa de Reticulação (também chamada de reticulação química acoplada à espectrometria de massa, CL-MS ou XL-MS) utiliza reagentes bifuncionais para unir covalentemente aminoácidos que ficam dentro de uma janela espacial definida. Após a reticulação, a digestão enzimática direcionada gera uma mistura de peptídeos lineares e reticulados. A espectrometria de massa então detecta e identifica essas espécies entreligadas, traduzindo-as em restrições de distância, parceiros de interação e informações específicas do local que podem ser inseridas em modelos estruturais. Como o XL-MS fornece restrições derivadas da proteômica, ele complementa a criomicroscopia eletrônica e a cristalografia de raios X ao aterrar densidades ambíguas e refinar interfaces.
Além de seu poder integrativo, a Espectrometria de Massa de Reticulação Cruzada oferece vantagens práticas: escala para alta capacidade, suporta aplicações intracelulares e não requer marcadores de fusão genética ou marcagem química especial. Crucialmente, a ligação cruzada covalente "congela" contatos fracos ou transitórios, tornando o XL-MS um parceiro potente para purificação de afinidade ou MS nativo quando o objetivo é revelar interações que, de outra forma, se dissipariam.
Por que a adoção demora: pontos persistentes de dor
Mesmo com benefícios claros, vários obstáculos ainda impedem a implantação rotineira:
-Enriquecimento e detecção. Peptídeos reticulados são tipicamente raros em relação aos peptídeos lineares. Sem um enriquecimento ou fracionamento cuidadoso, as taxas de identificação caem e a cobertura dos sites linkáveis se torna irregular.
-Pontuação e validação complexas. Masas precursoras compostas e padrões de fragmentação complexos complicam a interpretação do espectro. O controle da taxa de falsa descoberta (FDR) para pares cruzados requer pontuação consciente do local e limiares cuidadosamente ajustados, ou links espúrios podem passar despercebidos.
-Otimização química. A escolha e a dose do cruzamento são importantes. A superligação pode prejudicar arquiteturas nativas; a subreticulação gera mapas esparsos. A reticulação dentro da célula adiciona complexidade matricial que pode reduzir a recuperação de peptídeos.
-Projeto de método de instrumentos. A sensibilidade deve ser equilibrada com a qualidade da fragmentação. Se você usar apenas HCD, a cobertura de fragmentos pode ser desigual; ETD/EThcD precisa de calibração para garantir que os íons úteis sejam recuperados para muitos pares de peptídeos diferentes.
-Software e padrões fragmentados. Ferramentas heterogêneas e formatos de relatórios dificultam a comparação de resultados entre projetos ou a fusão de resultados XL-MS com bancos de dados estruturais para modelagem integrativa.
Perguntas Frequentes Práticas e Soluções Comprovadas para Espectrometria de Massa de Cross-Linking
- Como devo escolher uma cruz?-Linker para o meu sistema?
• Ajustar o comprimento do espaçador às distâncias de interação previstas e escolher grupos reativos alinhados com resíduos dominantes (químicas de direcionamento à lisina são comuns).
• Ajuste a dose piloto da concentração do reticulador e a duração da reação para evitar a superreticulação.
• Em matrizes complexas, escolha químicas com reatividade bem caracterizada e protocolos de têmpera validados.
- Como posso melhorar a recuperação do cruzado-Peptídeos ligados?
• Empregar fluxos de trabalho de digestão sequenciais (por exemplo, Lys-C e depois tripsina) para ampliar os limites dos peptídeos e diminuir clivages perdidos.
• Utilizar enriquecimento em nível peptídico junto com fracionamento ortogonal para focar espécies entreticuladas à frente da LC-MS.
- Que LC-As configurações da Microsoft aumentam as taxas de identificação? (Nenhum método LC-MS único serve para todos os peptídeos cruzados. A otimização de métodos deve ser considerada parte do fluxo de trabalho XL-MS, não uma configuração única.)
• Adquirir MS/MS de alta resolução e ajustar as energias de colisão para equilibrar a espinha dorsal e a fragmentação dos reticuladores.
• Considere fragmentação mista (HCD suplementado com ETD ou EThcD) para uma cobertura de sequência mais rica de pares cruzados.
- Como posso controlar descobertas falsas?
• Aplicar abordagens de alvo - isca adaptadas para buscas cruzadas e aplicar filtros de pontuação delta, nível de local e tipo de linkagem.
• Validar links críticos entre réplicas biológicas e técnicas e verificar com ensaios bioquímicos de densidade crio-EM ou ortogonais.
- A Espectrometria de Massa de Reticulação Cruzada pode capturar interações transitórias em células vivas?
•Sim - a reticulação realizada dentro das células preserva interações passageiras. Otimize a têmpera e a lise para integridade do aduto, e use o enriquecimento para gerenciar os efeitos da matriz antes da EM.
- Como faço para integrar XL-MS com criogenia-EM ou X-Ray?
• Fornecer limites de distância específicos do linker e métricas de confiança. Use restrições XL-MS para orientar domínios, confirmar interfaces e sinalizar regiões discordantes para refinamento do modelo.
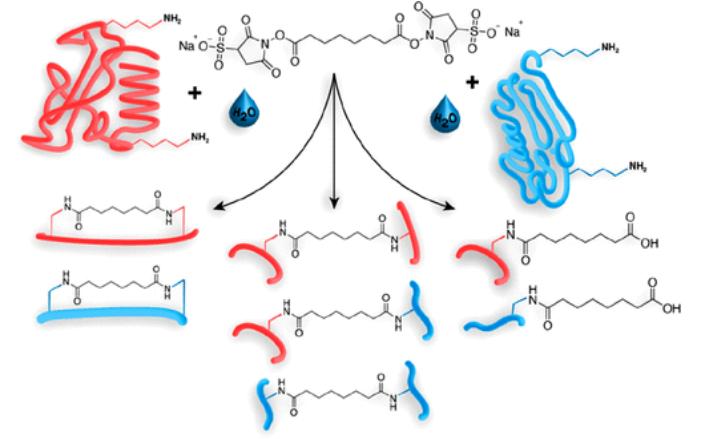
(Reação dos ésteres do NHS reativos a aminas, exemplificada para BS3 (painel superior).
Produtos de reação com proteínas incluem ligações cruzadas intrapeptídicas (Tipo 1; Esquerda),
Ligações Cruzadas Interpeptídicas (Tipo 2; Meio),
e Cruzamentos "Sem Saída" ou "Mono-links" (Tipo 0; Certo))
Uma pilha integrada de serviços e produtos que acelera o XL-MS
Oferecemos um Serviço XL-MS de ponta a ponta, abrangendo desenho experimental, otimização química, preparação de amostras, aquisição de LC-MS e interpretação de dados. Essa abordagem integrada minimiza o processo de tentativa e erro, reduz descobertas falsas e encurta o caminho dos experimentos piloto até resultados publicáveis. Os clientes podem enviar amostras pré-reconectadas ou co-projetar o fluxo de trabalho com nossa equipe desde o início.
- Por que nossas soluções genômicas e equipamentos de laboratório fortalecem XL-MS?
XL-MS se beneficia de preparação estável de amostras a montante e detecção robusta a jusante. Fornecemos instrumentos avançados, reagentes de alta qualidade e consumíveis que suportam a Espectrometria de Massa de Reticulação Cruzada e pipelines de câmbicos relacionados em ambientes acadêmicos, clínicos e industriais. Impulsionados por eficiência e precisão, nossos fluxos de trabalho suportam estudos de alta produtividade com qualidade de dados consistente – condições ideais para uma interpretação confiante de espectros peptídicos reticulados.
- Perfil de Interação ChIP-Seq e Cromatina
Quando projetos investigam contatos proteína-cromatina juntamente com a Espectrometria de Massa de Reticulação, o ChIP-seq adiciona contexto genômico específico do locus. Ao mapear fatores de transcrição e sítios de ligação de histonas em todo o genoma, o ChIP-seq ajuda a conectar as restrições do XL-MS a paisagens regulatórias funcionais, fortalecendo conclusões mecanicistas e orientando hipóteses para experimentos de acompanhamento.
- Genômica e Suporte à Preparação de Amostras
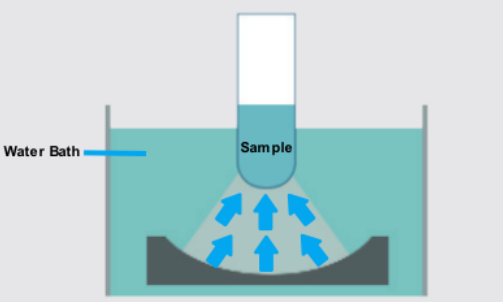
Longlight foca em biologia molecular e diagnóstico molecular com um portfólio de instrumentos e reagentes relacionados a NGS, incluindo soluções de ultrassonização focadas para preparação precisa de bibliotecas. Essas capacidades estabilizam a qualidade da amostra a montante – um fator frequentemente negligenciado do sucesso – de modo que a Espectrometria de Massa Cross-Linking produz resultados interpretáveis e reproduzíveis entre lotes e projetos.
- Consumíveis e kits que reduzem a variabilidade
Fornecemos géis pré-fabricados de agarose, catadores de ácidos nucleicos, tubos de Qubit, kits de extração de ácidos nucleicos e kits de preparação de biblioteca. O uso de consumíveis comuns e procedimentos operacionais padrão rigorosos reduz a variabilidade do dia a dia, ajudando as equipes a entregar desempenho estável XL-MS por meio de medições repetidas e integrações multi-ômicas.
- Recomendações Simplificadas para Prevenir Erros Comuns
• Executar titulações piloto para ajustar a concentração do reagente e o tempo de reação por matriz.
• Utilizar fluxos de trabalho padronizados de proteases e enriquecimento em nível peptídico para aumentar o rendimento de peptídeos reticulados.
• Mantenha as versões do método LC - MS registradas e, quando apropriado, favorize fragmentação híbrida de alta resolução HCD/ETD ou EThcD.
• Definir estritos de pontuação, delta-escore e filtros em nível de local, e reproduzir links prioritários em réplicas técnicas e biológicas independentes.
• Combinar Espectrometria de Massa de Reticulação Cruzada com crio-EM ou raios X e revelar limites de distância e métricas de confiança específicas do linker para modelagem integrativa.
Do Piloto à Escala: Seu Próximo Passo
Planejando Espectrometria de Massa de Reticulação para mapeamento de interações proteicas, validação de estruturas ou modelagem integrativa? Junte-se aos nossos especialistas para criar um fluxo de trabalho confiável e de alta produtividade, otimizado para seus objetivos. Aconselharemos sobre a seleção de cross-linkers, organizaremos o envio de amostras e realizaremos digestão, enriquecimento, aquisição de EM e análise de dados. Espere um relatório conciso com insights acionáveis. Colabore conosco para reduzir riscos, corrigir gargalos comuns e elevar o XL-MS de pilotos iniciais para uma descoberta confiável no dia a dia.