Postagem relacionada

Revisão da Exposição | O ARABLAB foi realizado com sucesso, ansioso para encontrá-lo novamente!
2025-02-25
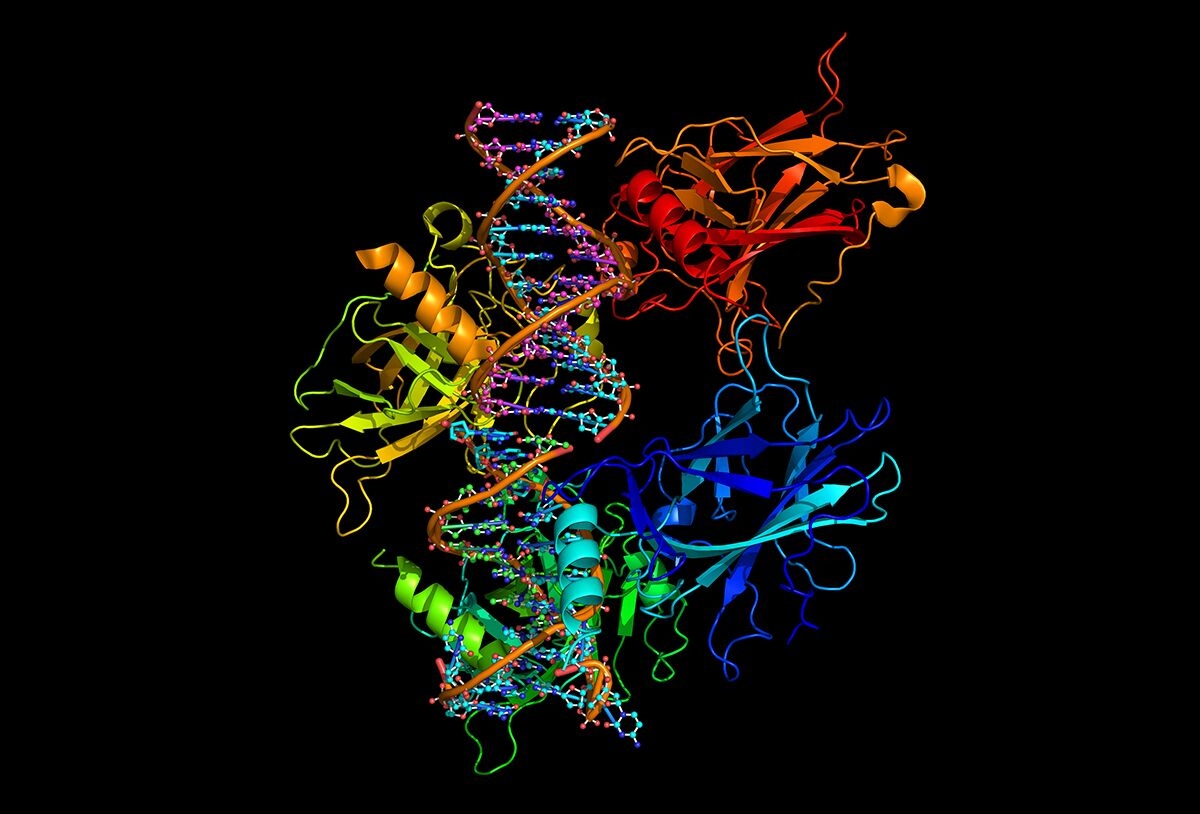
Despesas operacionais ocultas do equipamento de imagem de análise de proteínas
2025-08-20
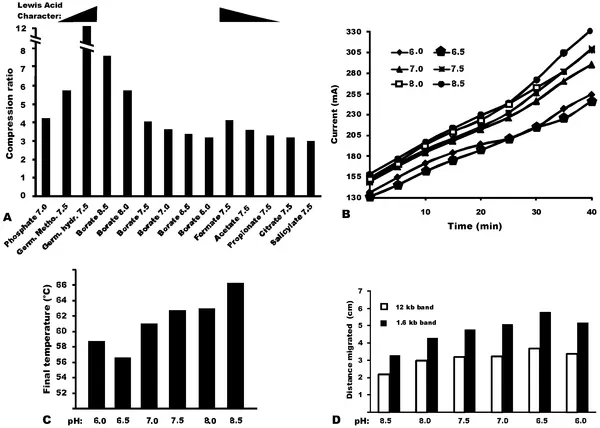
Buffer de DNA pré-fabricado fácil de usar: sem confusão de diluição, sem refrigeração, apenas géis de 5 minutos
2026-04-15
Solução de Problemas do ChIP-Seq 101: Corriga o Sinal Baixo Passo a Passo
2026-02-28A solução de problemas do ChIP-Seq geralmente começa com um sintoma simples — sinal baixo — mas as causas reais geralmente se espalham pela qualidade da cromatina, desempenho de anticorpos, condições de imunoprecipitação e controle de qualidade da biblioteca. Na Longlight Technology, apoiamos laboratórios que executam ChIP-Seq para marcas de histonas e fatores de transcrição, e vemos os mesmos "pontos de falha silenciosos" se repetirem entre diferentes instrumentos e tipos de amostras. Este guia básico de solução de problemas do ChIP-Seq guia os iniciantes passo a passo para recuperar o sinal em ordem lógica, usando checkpoints práticos que você pode verificar em uma única execução.
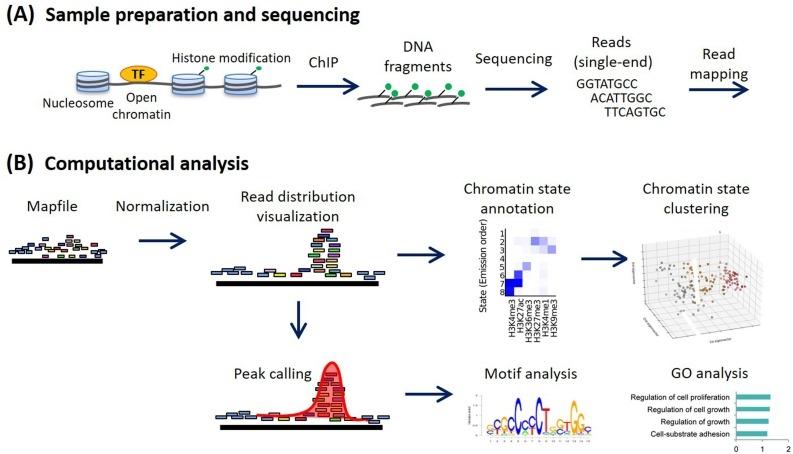
Métodos para análise ChIP-seq: Um fluxo de trabalho prático e aplicações avançadas - ScienceDirect
1) Definir "Sinal Baixo" Antes de você mudar qualquer coisa
Sinal baixo pode significar coisas diferentes: picos insuficientes, enriquecimento fraco em loci conhecidos ou uma biblioteca que parece boa, mas mapeia mal. Boa solução de problemas com ChIP-Seq começa rotulando claramente o modo de falha, pois cada modo aponta para correções diferentes.
Uma forma amigável para iniciantes de definir o problema é verificar três camadas:
✓ Camada de Biologia: O alvo está presente no seu estado celular (estimulado vs em repouso, estágio de diferenciação, momento do tratamento)?
✓ Camada de enriquecimento: O DNA ChIP mostra enriquecimento por qPCR em um locus controle positivo versus uma região negativa?
✓ Camada de sequenciamento: Você tem leituras únicas e mapeadas suficientes e um nível de duplicado razoável?
Se você não conseguir responder essas três, não "otimize tudo". Execute um experimento controlado primeiro: mantenha a amostra igual, mantenha a profundidade de sequenciamento modesta e altere apenas uma variável suspeita.
2) Comece com cromatina: tamanho do fragmento ae Controle de Perdas
Quando os laboratórios perguntam por que um ChIP "não funciona", a causa raiz mais comum é a cromatina que está fragmentada demais, subfragmentada ou simplesmente perdida durante a limpeza. No Troubleshooting ChIP-Seq, a cromatina é sua base — se for inconsistente, cada etapa posterior vira ruído.
Para fluxos de trabalho baseados em sonicação, muitos laboratórios buscam fragmentos na faixa de ~150–300 pb para chamadas de pico agudas e imunoprecipitação consistente. Se os fragmentos forem maiores, em sua maioria maiores (por exemplo, >500 pb), os anticorpos têm dificuldade em puxar os complexos-alvo de forma eficiente. Se os fragmentos forem muito pequenos, você pode destruir epítopos ou aumentar o fundo liberando DNA inespecífico.
Pontos práticos de verificação que você pode fazer imediatamente:
• Medir o DNA após a reconexão cruzada reversa e a limpeza (não apenas antes da IP). Uma grande queda aqui indica perda em contas/colunas ou condições adversas.
• Comparar perfis de fragmentação entre amostras. Se uma amostra estiver "perfeita" e a próxima estiver borrada ou superdimensionada, foque nas configurações de lise e sonicação, não no anticorpo primeiro.
• Manter uma alíquota de "DNA de entrada" de cada lote. Esse é seu ponto de partida tanto para qPCR quanto para o controle de qualidade de bibliotecas.
Na Longlight Technology, recomendamos tratar a preparação da cromatina como uma etapa controlada de fabricação: fixar a composição do tampão, manter a temperatura da amostra estável durante a sonicação e registrar as configurações exatas do ciclo. Pequenos desvios criam grandes diferenças na resistência máxima posteriormente.
3) Ajuste de Anticorpos: Especificidade, Variação do Lote, and Controles
Se a cromatina parecer razoável, o próximo passo na solução de problemas do ChIP-Seq é a seleção e validação de anticorpos. O baixo sinal geralmente é causado pelo uso de um anticorpo "bom para o ocidental", mas fraco para o ChIP, ou pela variabilidade de lote para lote.
Uma boa estratégia de anticorpos é construída em torno de controles:
✓ Alvo de controle positivo: uma marca de histonas com enriquecimento robusto (comumente usada para confirmar a saúde do fluxo de trabalho).
✓ Controle negativo: IgG ou um controle isotipo para estimar o pull-down de fundo.
✓ Loci conhecidos qPCR: um ou dois loci positivos publicados para o seu alvo, além de uma região desértica genética.
Para fatores de transcrição, o sinal pode ser inerentemente menor que as marcas de histonas. Isso significa que seu anticorpo deve ter alta afinidade e suas condições IP devem estar limpas. Se você é novo no TF ChIP, não comece mudando a profundidade de sequenciamento. Primeiro, confirme o enriquecimento por qPCR. Se o enriquecimento qPCR for fraco, mais leituras geralmente vão te dar mais ruído.
Dica prática: Quando você trocar de lote de anticorpos, verifique novamente o enriquecimento no mesmo lote de cromatina, se possível. Se a mudança de estacionamento quebrar o sinal, o fluxo de trabalho não é necessariamente "errado" — seu desempenho do reagente mudou, e seu caminho de solução de problemas deve refletir isso.
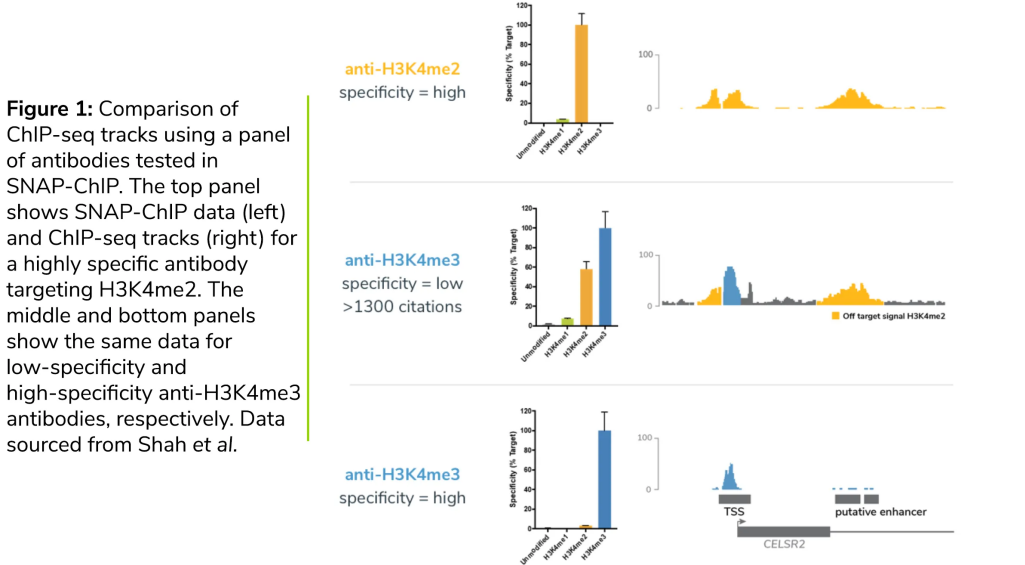
Escolhendo o Anticorpo ChIP Certo para o Seu Experimento - EpiCypher
4) Sequência limpa de otimização de IP — sem dúvidas
Além da cromatina e dos anticorpos, a química IP (esferas, lavagens, incubação) é o próximo ponto crítico. Sinal baixo costuma ser um problema de fundo.
✓ Seleção de contas: Escolha a proteína A/G que se encaixe na sua espécie/isótipo de anticorpos.
✓ Quantidade de anticorpos: Titule para evitar puxões fracos ou DNA inespecífico elevado.
✓ Balanço de lavagem: Calibre a stringência para remover ruído, mas preservando interações fracas, mas reais.
Uma regra prática para iniciantes é ajustar apenas um eixo por corrida:
• Se existirem picos, mas forem fracos, aumentar a captura efetiva (um pouco mais de anticorpos, melhor ligação das esferas, incubação mais longa).
• Se os picos forem largos e barulhentos, aumente a especificidade (lavagens mais fortes, melhor bloqueio, redução da sobrecarga de anticorpos).
Do ponto de vista do fabricante, a Longlight Technology projeta reagentes de imunoprecipitação e sistemas de esferas magnéticas para minimizar a perda durante o manuseio, porque a perda de amostras é exatamente como "sinal baixo". Separação suave das contas, fixação consistente e passos de lavagem limpa reduzem a variabilidade entre os operadores — especialmente importante para equipes que treinam novos funcionários.
5) Controlo de qualidade da biblioteca: Quando "Bom DNA" Ainda dá sinal baixo
Às vezes, o enriquecimento de DNA ChIP é real, mas os dados finais ainda parecem planos. Na solução de problemas ChIP-Seq, isso geralmente aponta para métricas de construção de bibliotecas ou sequenciamento.
Causas comuns de baixo sinal em nível de biblioteca:
✓ Amplificação excessiva: muitos ciclos de PCR podem inflar duplicados e reduzir leituras únicas utilizáveis.
✓ Artefatos adaptadores/primer: eles consomem leituras de sequenciamento sem melhorar a cobertura do alvo.
✓ Complexidade pobre: frequentemente causada por entrada muito baixa de DNA ChIP ou perda durante a limpeza.
O que verificar antes de refazer todo o ChIP:
• Distribuição do tamanho da biblioteca (você quer um pico limpo, não múltiplos picos inesperados).
• Taxa de duplicação e taxa de mapeamento única após o alinhamento.
• Fração de leituras em picos (FRiP) tendência em relação à sua linha de base interna (até iniciantes conseguem acompanhar "melhor vs pior" ao longo das corridas).
Se você suspeita de superciclagem da biblioteca, uma melhoria simples é reduzir a contagem de ciclos e aumentar a eficiência da captura a montante (melhor recuperação de cromatina e especificidade de IP). Sequenciar mais profundamente não pode compensar uma biblioteca de baixa complexidade.
6) Passo-Por-Recuperação do Step Signal Você Pode Começar Amanhã
Uma sequência prática que supera ajustes ad hoc:
✓ Passo 1: Verificar se os fragmentos de cromatina estão a ~150–300 pb e confirmar a recuperação de DNA após a cruzamento reversa.
✓ Passo 2: Verifique o enriquecimento por qPCR em um locus positivo e um negativo antes da preparação da biblioteca.
✓ Passo 3: Adicionar controles adequados (entrada IgG) para separar "sem enriquecimento" de "alto fundo".
✓ Passo 4: Ajuste as condições IP uma variável de cada vez (contas, quantidade de anticorpos, stringência de lavagem).
✓ Passo 5: Audite métricas de biblioteca (duplicação, mapeamento, distribuição de tamanho) antes de assumir que a profundidade de sequenciamento é o problema.
CTA (Tecnologia Longlight): Se quiser um caminho mais rápido, entre em contato com a Longlight Technology para uma lista de verificação de solução de problemas ChIP-Seq e uma folha de diagnóstico amostra por amostra (biblioteca → de de cromatina → IP). Também podemos recomendar uma estratégia de design de controle e pareamento de reagentes para reduzir a variabilidade do operador e ajudar iniciantes a alcançar um enriquecimento estável mais cedo.
Sinal baixo é frustrante, mas raramente é misterioso. Com um fluxo disciplinado de solução de problemas ChIP-Seq — começando pela integridade da cromatina, depois ajuste de anticorpos, depois especificidade IP e, finalmente, controle de qualidade de biblioteca — você pode transformar uma execução fraca em um protocolo repetível que escala entre amostras, equipe e projetos.